研究介绍
染色质结构及转录
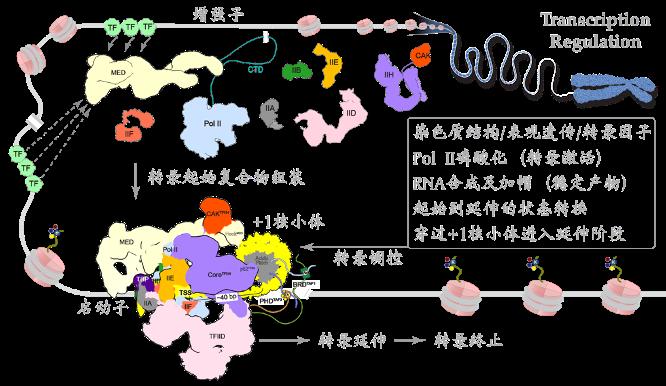 以人类为代表的高等生物进化出一系列复杂的基因表达调控机制,利用同一套基因组形成多种不同表型的细胞,实现复杂的生长发育过程。发生在基因启动子区的转录起始过程是基因表达调控的核心。通过表观遗传修饰(如启动子区DNA甲基化),染色质重塑暴露启动子DNA,在启动子区装配超大分子量转录起始复合物,细胞可在复杂的转录调控信号作用下实现基因差异性表达,从而决定细胞的命运,并影响众多的生理病理过程,对上述复杂过程的分子机制的研究,是基本生命科学问题,极具挑战性。
以人类为代表的高等生物进化出一系列复杂的基因表达调控机制,利用同一套基因组形成多种不同表型的细胞,实现复杂的生长发育过程。发生在基因启动子区的转录起始过程是基因表达调控的核心。通过表观遗传修饰(如启动子区DNA甲基化),染色质重塑暴露启动子DNA,在启动子区装配超大分子量转录起始复合物,细胞可在复杂的转录调控信号作用下实现基因差异性表达,从而决定细胞的命运,并影响众多的生理病理过程,对上述复杂过程的分子机制的研究,是基本生命科学问题,极具挑战性。
我们建立了体外重构转录起始超大复合物的独特方法,结合生物化学和结构分析,解决了转录起始领域若干关键问题。揭示染色质重塑复合物结合核小体机制,提出启动子上核小体剔除(转录起始所必须)模型(Science,2020a);揭示了转录起始复合物的启动子识别、分步组装、转录激活等多个过程的分子机制,阐明为什么转录可以在各种不同的启动子上开始(Science,2021a;Science,2021b,cover);揭示+1位核小体(启动子下游的第一个核小体上)对转录起始过程的调控机制,为研究表观遗传和基因表达调控提供新的指导框架和结构基础(Science, 2022);发现并鉴定新型转录调控复合物,揭示其对转录起始的抑制作用(Science,2020b)。部分成果入选“中国生命科学十大进展”。
揭示转录起始复合物识别启动子及动态装配的分子机制
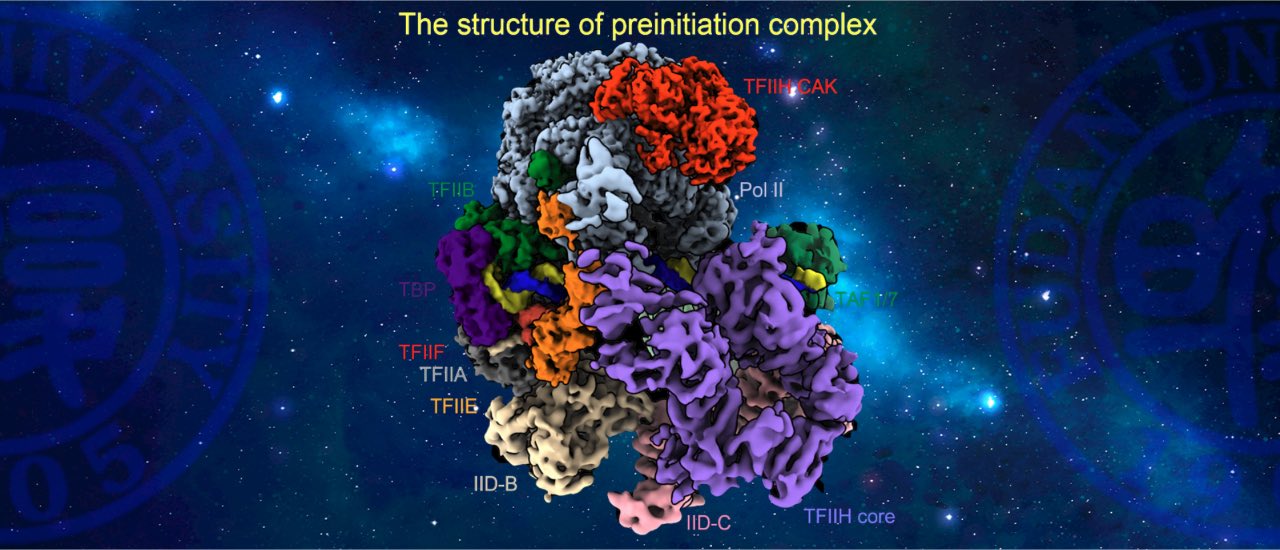
转录起始过程发生在几乎所有编码基因和大部分非编码基因的启动子区,是基因表达调控的核心,以RNA聚合酶II为核心的转录起始复合物(PIC)可识别基因的启动子并进行分步骤装配,完整复合物包含50余个蛋白质,分子量达2.6MDa,起始基因的转录。其中识别启动子的TFIID复合物是整个装配过程的关键,由14种共20个亚基组成,分子量达1.3MDa。
我们报道了包含TFIID的完整PIC结构,揭示了PIC如何识别不同类型启动子并完成多步装配的完整动态过程(Science,2021a)。研究发现TFIID含有多个DNA结合区,具有较高的序列包容度,可识别各种不同类型的基因启动子。TFIID招募聚合酶和多个通用转录因子逐步装配成完整PIC复合物。令人意外的是,在PIC复合物中,TBP以同样的方式弯折TATA box(存在于~15%基因)和TATA-less(存在于~85%基因)启动子,很好解释了PIC装配和基因转录为何可发生在几乎所有类型启动子上。针对不同类型启动子,PIC通过两种方式将启动子推动至聚合酶催化中心上方准备转录,提出two-track promoter deposition模型。第一种为“三步到位”,既PIC装配过程产生Park,Neutral,Drive三种启动子构象逐步到位。第二种为“直接到位”,既在装配早期就形成Drive构象启动子并一直维持到装配完成。“三步到位”方式有可能作为检查点以避免非必要情况下的转录发生。组装完成的PIC,为转录起始做好了两方面准备。CDK7激酶磷酸化聚合酶的C端结构域(CTD),是转录起始的关键调控步骤。启动子到位后可通过PIC中解旋酶使模板链DNA进入聚合酶催化中心开始转录。该项工作在分子水平上展示了高度动态的转录起始过程,为后续研究基因表达调控奠定了理论基础。
揭示转录起始连续动态全过程
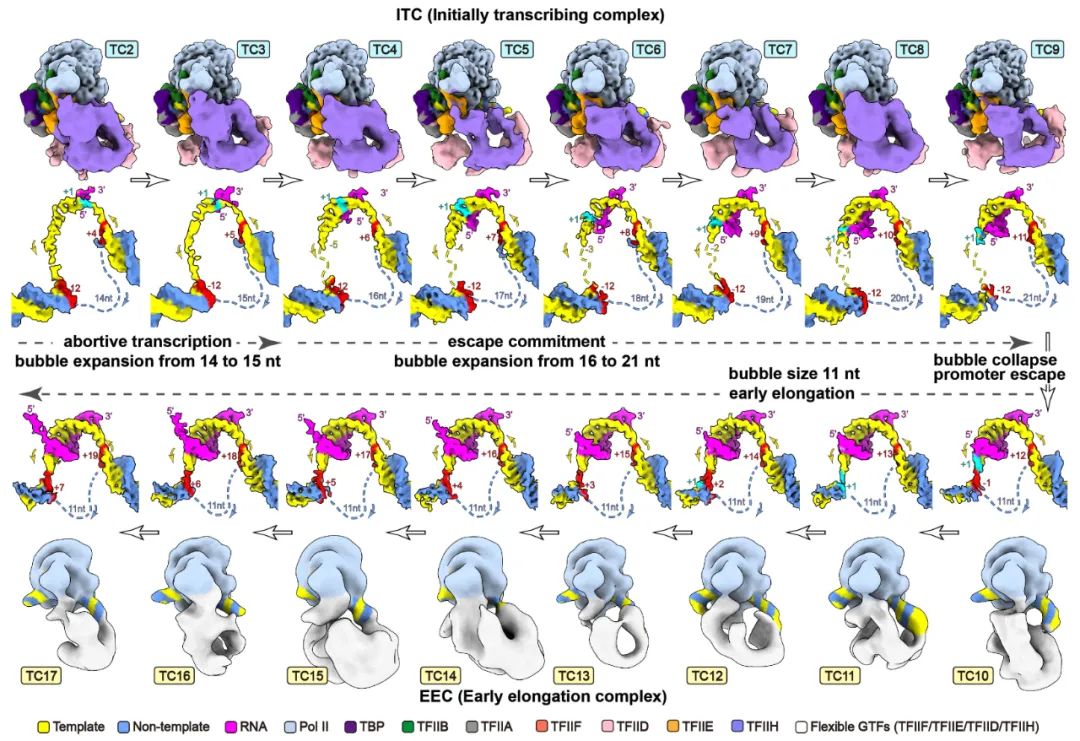
RNA聚合酶II(Pol II)本身不具备结合和打开基因启动子的能力,需要与6个通用转录因子(general transcription factors,GTFs)包括TFIID、TFIIA、TFIIB、TFIIF、TFIIE以及TFIIH共同在启动子上组装形成转录前起始复合物(preinitiation complex,PIC),才能起始转录。在ATP的驱动下,TFIIH将转录起始位点附近的DNA双链打开,模板链进入Pol II的活性中心,PIC转变形成了初始转录复合物(initially transcribing complex, ITC);随后,Pol II以NTP为底物,催化合成RNA,期间经历一系列复杂的结构和复合物组成变化,ITC转变形成早期延伸复合物(early elongation complex, EEC),进入后续的延伸过程。以往众多生化实验描绘出了转录起始的大致过程,但由于实验设计和实验材料的不一致,不同的实验结论之间相互矛盾,许多结论长期以来未得到统一。
我们将转录反应人为的暂停在转录起始位点下游2-17位核苷酸的位置,首次用结构重现出了转录从头起始的16个连续动态全过程,揭示了通用转录因子(GTFs)和转录泡协同RNA聚合酶Pol II调控转录起始向转录延伸转变的分子机制 (Science, 2023)。将过去几十年来数百篇关于转录起始研究中的众多看似矛盾的结论作了统一。回答了起始过程中众多核心问题,揭示了转录起始调控的机制,为理解基因表达调控奠定了结构基础。
完整PIC-Mediator转录前起始复合物结构与功能

Mediator可以将不同信号通路的转录激活信号,传递到PIC上激活转录。体外实验表明,Mediator结合PIC和众多转录因子,促进启动子区PIC复合物的组装并激活TFIIH上的CDK7激酶活性,促进Pol II羧基端结构域(Pol II CTD)的磷酸化,极大的提升PIC的转录活性。Mediator由26个蛋白所组成,分子量1.5兆道尔顿(MDa)。基于TFIID的完整PIC与Mediator组成转录起始超级复合物(称为PIC-Mediator),具备转录起始过程所有因子和完整的基本转录活性(basal transcription)。几乎所有转录因子及转录调控因子都是通过作用在PIC-Mediator复合物上激活转录起始。
我们报道了首个结构与功能完整的PIC-Mediator复合物(Science,2021b,cover),揭示了PIC-Mediator的动态组装过程以及Mediator调控Pol II CTD磷酸化的分子机制。解析了人源Mediator复合物近原子分辨率的冷冻电镜结构,发现Mediator的Tail模块可呈现延展构象(Extended)和弯折构象(Bent),表明Mediator本身的动态性。发现结合PIC时Mediator发生模块重排(modular reorganization),头部的HB1亚模块和Knob亚模块夹住Pol II CTD的两段多肽链,形成“三明治”结构,稳定Pol II CTD并将其送至CDK7活性中心进行磷酸化反应,提出“CTD磷酸化门控”模型,使CTD结合在Mediator上,保证有效且持续地被磷酸,而完全磷酸化后又使PIC与Mediator解离。TFIID赋予了PIC-Mediator结构和功能的完整性。在PIC-Mediator整体结构中,Mediator和TFIID分别位于TFIIH的上下两面,两者共同结合并稳定TFIIH,使TFIIH中CDK7激酶和XPB移位酶在PIC-Mediator中正确定位并发挥活性。其中XPB推动启动子DNA进入Pol II催化中心开始转录,CDK7磷酸化Pol II的CTD允许Pol II聚合酶离开启动子区进入转录延伸,二者的活性是转录起始所必须的。说明TFIID在PIC-Mediator超大转录起始复合物的组装和发挥功能中的关键作用。
揭示+1核小体调控转录起始的分子机制
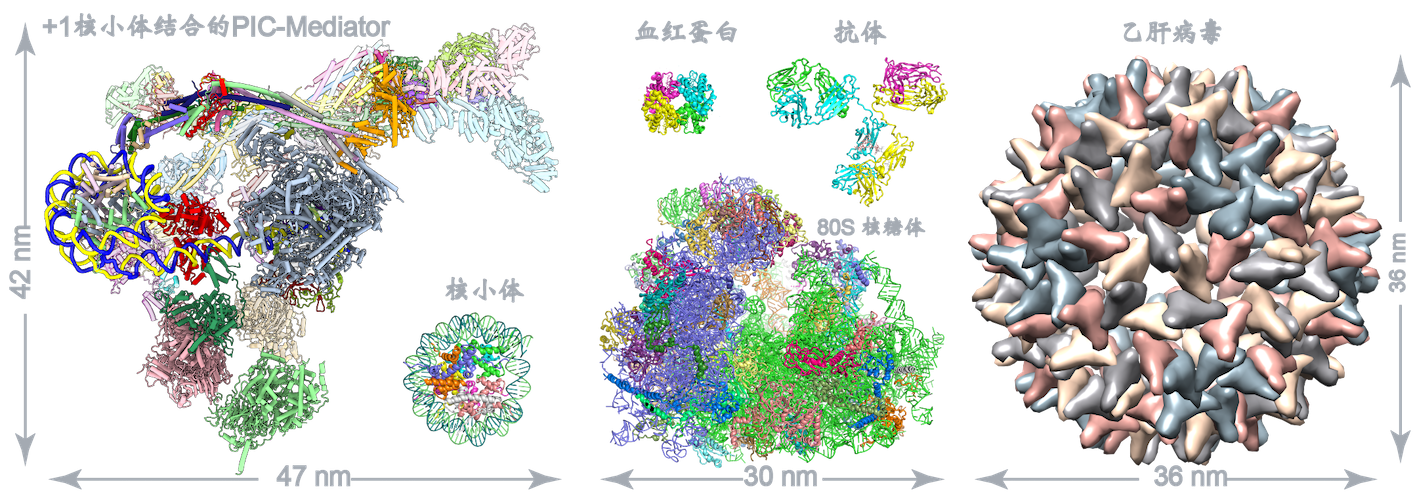
PIC-Mediator是转录起始调控的核心,基因表达主要受转录因子和表观遗传调控。其中转录因子结合在增强子和启动子附近促进PIC-Mediator的招募和组装,而表观遗传对转录的调控集中在启动子下游的第一个核小体上(称为+1核小体),是表观遗传调控的核心。我们解析了包含+1核小体的PIC-Mediator复合物结构,首次展示了转录起始复合物与+1核小体的紧密结合,表明+1核小体对转录起始复合物在染色质上组装的重要调控作用,建立了表观遗传和转录起始的直接关联(Science,2022)。
目前主流观念认为,转录机器在进入到延伸阶段才会碰到核小体,该项工作首次在分子水平上展示出了转录起始复合物与+1核小体的紧密结合,将转录起始位点附近的表观遗传信号和转录起始建立了直接关联。改变了我们对转录起始过程和染色质相互关系的传统看法,为研究表观遗传和基因表达调控提供新的指导框架和结构基础。
发现并鉴定新型转录调控复合物INTAC并揭示其调控转录的机制
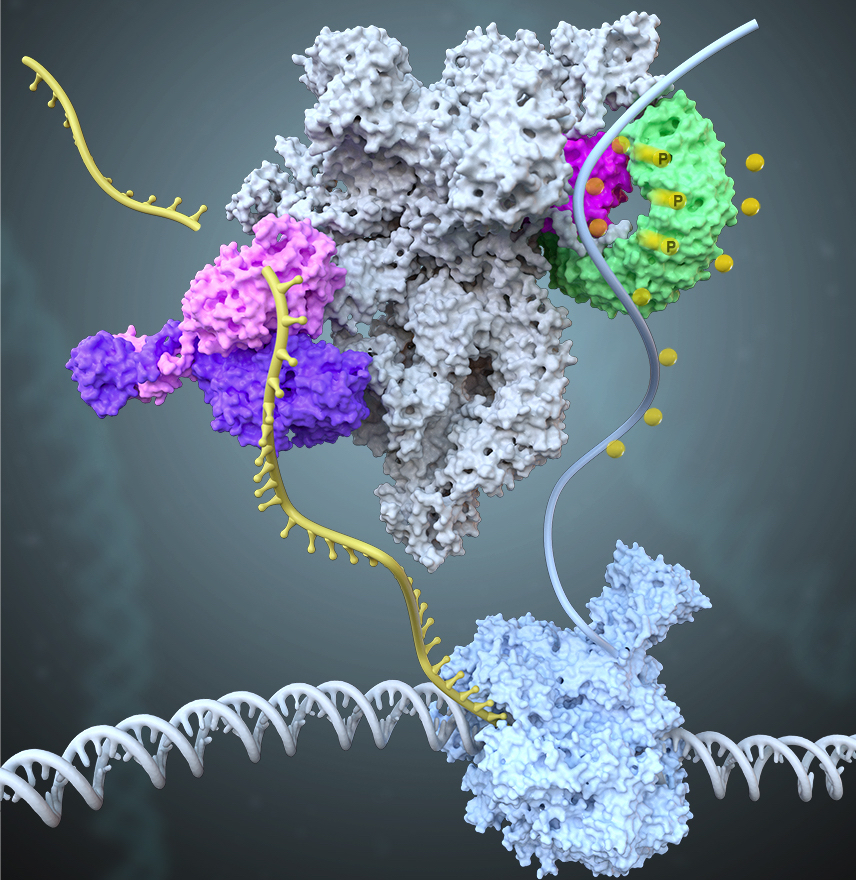
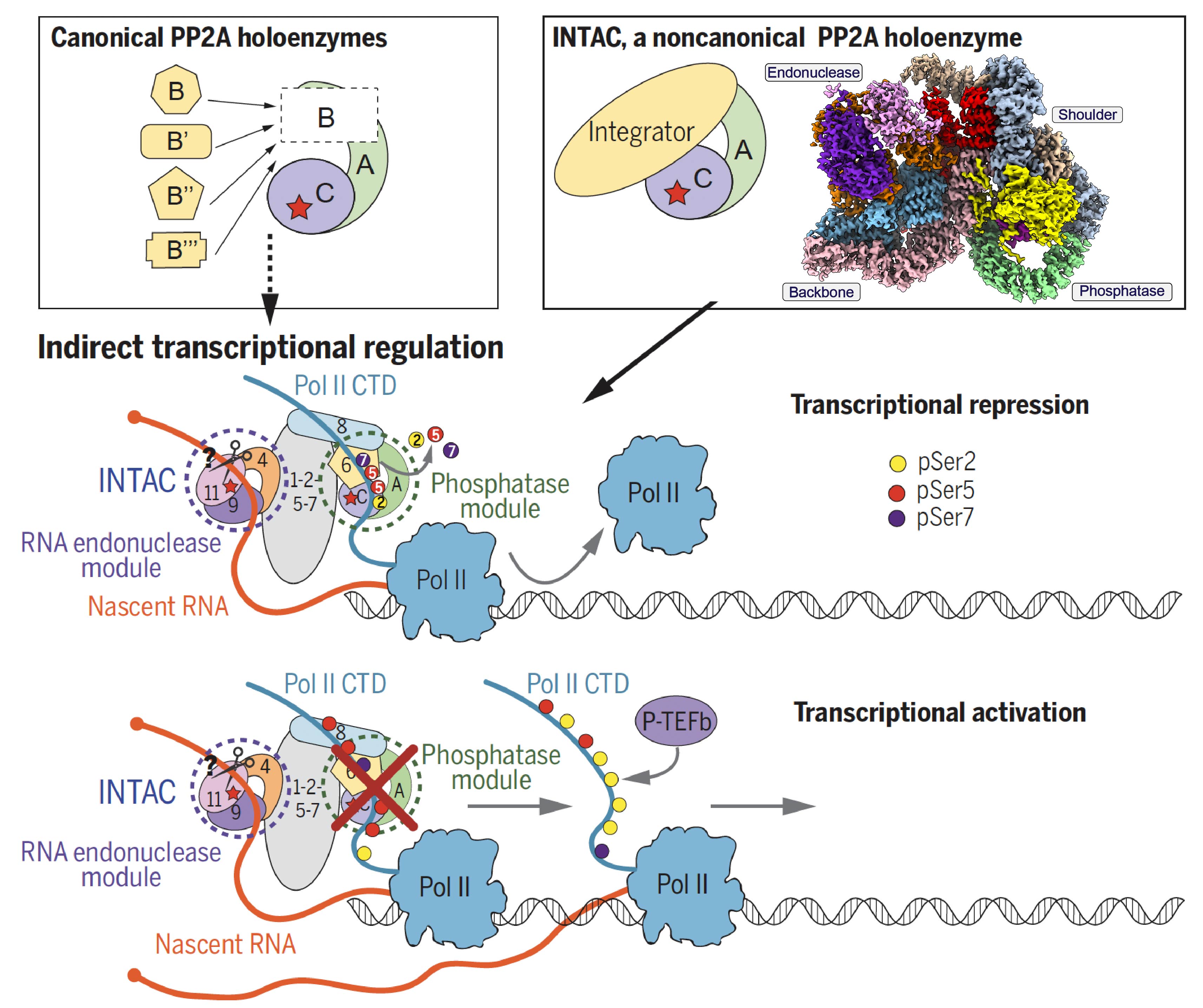
人类RNA聚合酶Pol II的CTD结构域含有52个七肽重复,每个七肽的第五位丝氨酸(Ser5)可被CDK7磷酸化启动转录,而Ser5去磷酸化是由转录起始进入转录延伸的关键,但其机制却知之甚少。我们与陈飞课题组合作,发现了一个全新的转录调控复合物INTAC,该复合物含有16个亚基,分子量近1.5 MDa(Science,2020b)。发现INTAC含有核酸内切酶和蛋白磷酸酶模块,分布在复合物两侧并分别调控转录的不同过程。其中蛋白磷酸酶模块来源于PP2A,是细胞内最主要的蛋白磷酸酶,但之前没有关于PP2A直接调控转录的报道。PP2A可去除聚合酶CTD多个位点的磷酸化进而抑制整体转录水平。而核酸内切酶剪切RNA终止启动子附近的非正常转录。该项工作证明PP2A在INTAC复合物中直接调控基因转录,将转录调控和PP2A两个重要领域建立了直接关联。
染色质重塑复合物结构及重塑机制研究
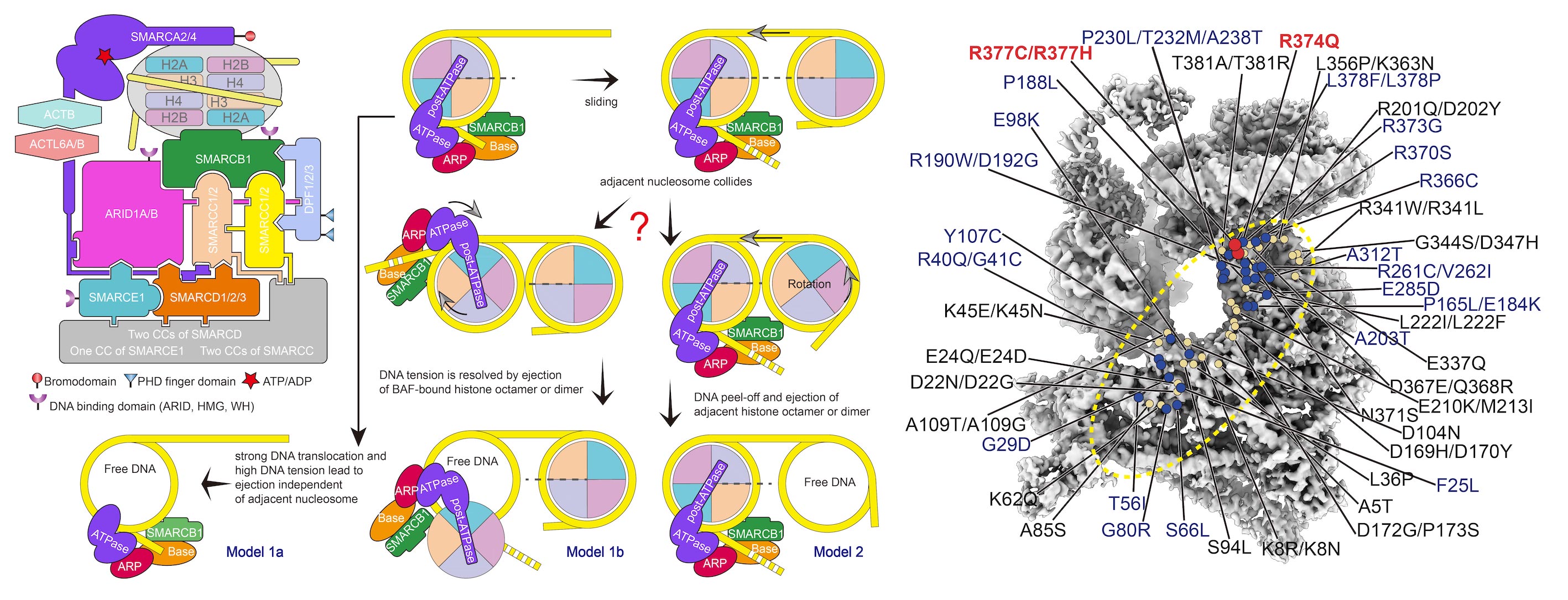
染色质重塑是染色质最核心的动态调控之一,而SWI/SNF家族重塑复合物具有独特的核小体剔除的功能,是几乎所有基因转录所必需。BAF/PBAF是哺乳动物SWI/SNF家族的染色质重塑复合物,其失调存在(>20%)多种肿瘤。以往的SWI/SNF家族复合物结构研究都局限在酵母体系,并且分辨率较低,这些研究始终无法代替人源SWI/SNF复合物结构,尤其是对理解疾病发生关联性的理解急需解析高分辨人源SWI/SNF复合物结构。
我们解析了首个人源BAF复合物结合核小体的近原子分辨率结构(Science,2020a)。该结构作为哺乳动物BAF复合物的第一个冷冻电镜结构,也是SWI/SNF家族复合物结构中分辨率最高的。这一结构揭示了BAF复合物的组装以及核小体识别的机制,并且在这种独特的核小体识别模式的基础上,提出了BAF执行核小体剔除功能的机制模型。
这项工作将核小体识别、关键亚基的高频突变以及肿瘤发生联系起来,为理解SWI/SNF家族蛋白突变与癌症的关系打开了通道,为BAF亚基突变的致癌机制研究及靶向药物研发提供理论依据。该项研究呈现了染色质重塑领域内期待已久的高分辨BAF-核小体结构,结构信息可帮助理解BAF突变关联的癌症发生,并为癌症关联的染色质重塑机制的深入研究起到重要的推动作用。
团队成员

徐彦辉
发表论文
Structural insights into human Pol III transcription initiation in action
Structure of the human TIP60 complex
Structural insights into histone exchange by human SRCAP complex
Interplay between the transcription preinitiation complex and the +1 nucleosome
Structural visualization of transcription initiation in action
Structural basis of INTAC-regulated transcription
Structure of the SNAPc-bound RNA polymerase III preinitiation complex
Structures of +1 nucleosome–bound PIC-Mediator complex
Structural insights into assembly of transcription preinitiation complex
Structure of nucleosome-bound human PBAF complex
Structures of the human Mediator and Mediator-bound preinitiation complex
Structural insights into RNA polymerase III-mediated transcription termination through trapping poly-deoxythymidine
Structure of human RNA polymerase III elongation complex
Structure of the human RNA polymerase I elongation complex
Structure of nucleosome-bound human BAF complex
Identification of Integrator-PP2A complex (INTAC), an RNA polymerase II phosphatase
Structural insight into substrate preference for TET-mediated oxidation
Crystal Structure of TET2-DNA Complex: Insight into TET-Mediated 5mC Oxidation
PHD Finger Recognition of Unmodified Histone H3R2 Links UHRF1 to Regulation of Euchromatic Gene Expression
Crystal structure of PHD domain of UHRF1 and insights into recognition of unmodified histone H3 arginine residue 2
Structural insights into a dual-specificity histone demethylase ceKDM7A from Caenorhabditis elegans
研究动态
联系方式
上海市浦东新区张江路88号
上海梧桐岛生命科学研究院