Genome Medicine | 王晨飞课题组开发单细胞代谢状态及调控因子预测算法MetroSCREEN
细胞代谢具有显著的可塑性,能够适应生长与稳态的需求【1】。在肿瘤等病理条件下,微环境常呈酸性且营养匮乏,这些变化深刻影响代谢通路与信号网络,扰乱代谢调控因子的表达,并引发广泛的代谢重编程【2】。其中一个典型例子是瓦伯格效应:恶性细胞即使在有氧条件下,仍偏好通过糖酵解获取能量并大量产生乳酸【3】,以满足快速增殖的代谢需求。此外,肿瘤微环境(TME)中的免疫细胞与基质细胞也会发生相似的代谢适应,影响其成熟、活化及整体功能【4,5,6】。尽管对恶性细胞的代谢研究已较深入,但关于肿瘤微环境中基质细胞与免疫细胞的代谢亚型仍缺乏系统性研究。更为重要的是,对代谢重编程的调控机制与关键驱动因子的系统阐明依然不足,而这对于开发潜在的治疗干预至关重要。

2025年12月19日,同济大学生命科学与技术学院/上海梧桐岛生命科学研究院王晨飞团队在Genome Medicine上发表了文章Reference-guided computational framework identifies microenvironment metabolic subtypes and targets using pan-cancer single-cell datasets。该研究开发了基于单细胞转录组数据预测细胞代谢状态及其上游调控因子的方法MetroSCREEN(https://github.com/wanglabtongji/MetroSCREEN)。MetroSCREEN 通过快速富集算法量化反应级代谢活性,在参考内在的基因调控信号与外在的细胞间相互作用信号的基础上,采用以Pareto效率和稳健秩乘积为核心的多证据排序方案整合多源信息,最后通过基于约束的因果发现模块以推断代谢调控的方向性(图1)。
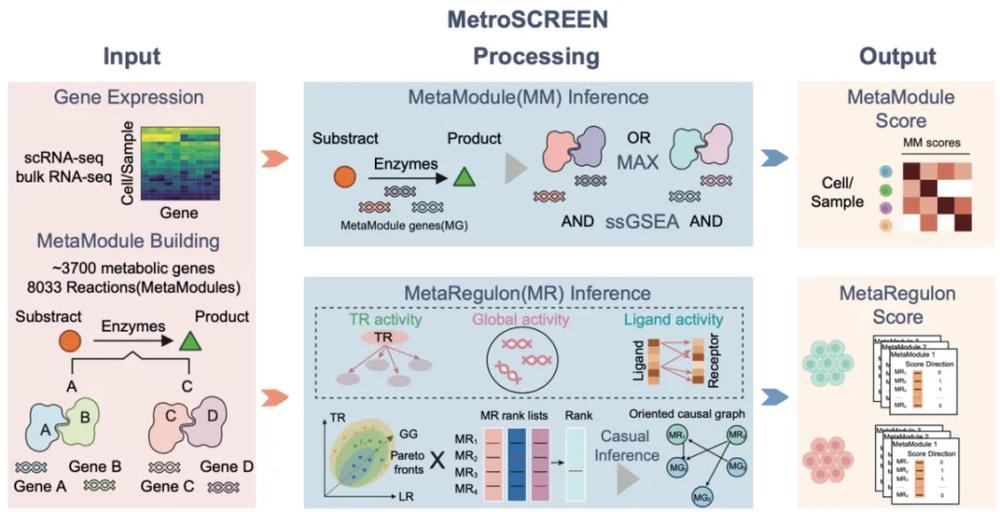
图1 MetroSCREEN的模型框架
研究人员将 MetroSCREEN 应用于泛癌单细胞数据【7】,构建了成纤维细胞和髓系细胞的泛癌代谢图谱 MetroTIME(http://wanglab-compbio.cn/MetroTIME/)。该图谱描绘了肿瘤微环境中关键基质与免疫代谢亚型的独特能量利用模式及其相关生物学特征(图2)。MetroTIME结果显示:成纤维细胞的细胞外基质重塑与糖酵解密切相关;在巨噬细胞中,鞘脂代谢与抗原呈递/吞噬功能高度耦联,并据此确定了相应的上游调控因子。进一步地,研究人员评估了这些代谢亚型及其调控因子的临床关联性,并将其与患者生存结局、免疫治疗反应及药物耐受性相联系。总体而言,该研究基于富集算法和多源信息整合策略,提出了一种可用于识别代谢亚型及其上游调控因子的方法。基于泛癌尺度的单细胞公共数据,系统阐明了跨肿瘤类型存在的代谢亚型及其调控靶点,为未来的代谢靶向抗癌治疗提供了可操作的候选靶点与策略。
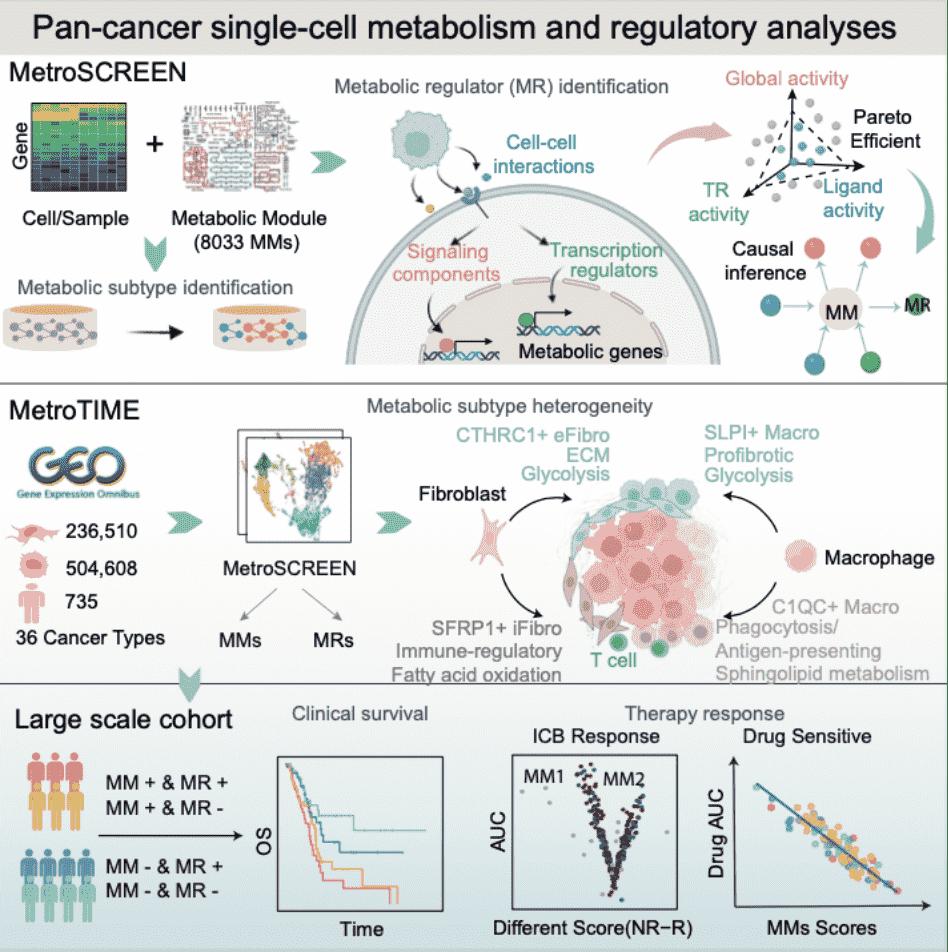
图2 MetroTIME研究框架的主要发现和下游应用
同济大学生命科学与技术学院/上海梧桐岛生命科学研究院王晨飞教授和同济大学生命科学与技术学院吴秋助理教授为该论文共同通讯作者,同济大学生命科学与技术学院博士研究生唐珂、博士后韩雅为文章的共同第一作者,并得到了上海市肺科医院张鹏教授、张乐乐副研究员,以及四川大学华西口腔医院李太文副研究员的大力支持。该研究得到了科技部、国家自然科学基金委、上海市科委等项目的重要支持。
参考文献:
-
Faubert, B., Solmonson, A. & DeBerardinis, R. J. Metabolic reprogramming and cancer progression. Science 368, eaaw5473 (2020).
-
Lyssiotis, C. A. & Kimmelman, A. C. Metabolic Interactions in the Tumor Microenvironment. Trends Cell Biol. 27, 863–875 (2017).
-
Koppenol, W. H., Bounds, P. L. & Dang, C. V. Otto Warburg’s contributions to current concepts of cancer metabolism. Nat. Rev. Cancer 11, 325–337 (2011).
-
Ghesquière, B., Wong, B. W., Kuchnio, A. & Carmeliet, P. Metabolism of stromal and immune cells in health and disease. Nature 511, 167–176 (2014).
-
Cassetta, L. et al. Human Tumor-Associated Macrophage and Monocyte Transcriptional Landscapes Reveal Cancer-Specific Reprogramming, Biomarkers, and Therapeutic Targets. Cancer Cell 35, 588-602.e10 (2019).
-
Gentles, A. J. et al. The prognostic landscape of genes and infiltrating immune cells across human cancers. Nat. Med. 21, 938–945 (2015).
-
Han, Y. et al. Spatiotemporal analyses of the pan-cancer single-cell landscape reveal widespread profibrotic ecotypes associated with tumor immunity. Nat. Cancer 1–19 (2025) doi:10.1038/s43018-025-01039-5.
原文链接:https://link.springer.com/article/10.1186/s13073-025-01572-z